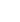硝酸銅是一種重要的無機化合物,化學式為Cu(NO3)2,通常以水合物形式存在(如三水合硝酸銅Cu(NO3)2·3H2O)。這種藍色結晶固體易溶于水和乙醇,在潮濕空氣中容易潮解,需要密封保存。作為過渡金屬硝酸鹽,硝酸銅在工業生產和實驗室中都具有廣泛用途,其水溶液呈現弱酸性(pH約4-5),與堿反應會生成氫氧化銅沉淀。
從物理性質來看,無水硝酸銅為白色粉末(密度2.32g/cm3),而常見的水合物則呈現誘人的藍綠色。特別值得注意的是其熱分解特性,當加熱至170℃以上時會逐步分解為氧化銅、二氧化氮和氧氣。這種化合物在氧化還原反應中表現出色,其標準電極電勢為+0.34V(Cu2+/Cu),這使得它成為許多化學反應的理想催化劑或氧化劑。
工業生產中通常采用銅或氧化銅與硝酸反應來制備硝酸銅,反應過程中會產生氮氧化物廢氣,需要配備完善的尾氣處理系統。在實驗室條件下,通過電解法也能制得高純度產品。由于其分子中含有硝基和銅離子,這種化合物兼具氧化性和配位能力,能與氨水形成深藍色的銅氨絡合物[Cu(NH3)4]2+。
硝酸銅在現代工業中扮演著多重角色,既可用于陶瓷釉料著色,又能作為紡織品媒染劑。在電子工業中,其溶液常用于印制電路板的蝕刻工序。農業領域則利用其殺菌特性配制波爾多液(與石灰混合),用于防治作物病害。需要特別注意的是,作為二級氧化劑,硝酸銅與可燃物接觸可能引發火災,操作時需穿戴防護裝備,避免吸入粉塵或接觸皮膚。
從安全角度考量,硝酸銅被歸類為環境有害物質,其對水生生物的毒性尤為突出(LC50約5mg/L)。儲存時應遠離有機化合物和還原劑,最好放置于陰涼通風處。廢棄處理需遵守當地環保法規,通常采用氫氧化鈉溶液中和后沉淀回收銅離子。隨著綠色化學的發展,研究人員正在探索更環保的替代品來減少硝酸銅在某些領域的應用。